Doses fracionadas da vacina
Especialistas veem uma luz no fim do túnel quando se trata de uma antiga discussão: diminuir a dose da vacina, mas mantendo a mesma taxa de imunogenicidade. O assessor científico sênior de Bio-Manguinhos, Akira Homma, que também vem participando dessas negociações, explicou que, em 1988, foi feito em um pequeno grupo de adultos um estudo para verificar com que quantidade de vacina havia resposta de proteção efetiva contra a doença e constatou-se que a vacina poderia ser utilizada em doses mais baixas do que as usuais.
Um outro estudo, com amostragem maior, foi realizado em adultos em 2013. Nesta ocasião, confirmou-se que a vacina é eficaz e segura com doses 10 vezes menores. “O que estamos querendo fazer agora é um grande estudo em crianças e saber a quantidade mínima de componente ativo necessária para protegê-las”, detalhou. Segundo o artigo da The Lancet, a OMS deve considerar a utilização da formulação existente por injeção subcutânea de uma dose reduzida de 0,5 ml a 0,1 ml, expandindo a oferta em cinco vezes.
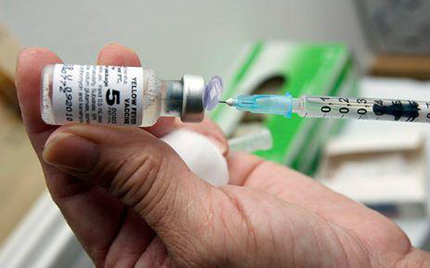
Especialistas sugerem uma dose reduzida de 0,5 ml a 0,1 ml da vacina.
Imagem: OMS
Está em discussão o financiamento deste estudo, devido a sua importância, entre a Fundação Bill & Melinda Gates, GAVI e a PATH. “Ainda não sabemos detalhes sobre quantas crianças serão necessárias, de onde ou sua faixa etária. No entanto, entendemos sua emergência”, concluiu Akira Homma.
Um outro trecho do artigo relata que não há, no entanto, a aceitação regulamentar de uma mudança de dosagem. “Um problema importante é a estabilidade e a data de validade, o qual é determinado por titulação do vírus em cada uma das formulações dos fabricantes de vacinas. Outra é se a duração a longo prazo de imunidade possa ser afetada pela dose mais baixa, embora este não seja um obstáculo para a utilização de emergência. Um terceiro problema é a eficácia da dose mais baixa em crianças, o que não foi determinada por testes clínicos. Mesmo assim, a OMS pode considerar e recomendar o uso de 0,1 ml de vacina utilizando o procedimento Emergency Use Assessment and Listing Procedure (EUAL), que foi invocado para permitir o uso de produtos não licenciados contra ebola durante a crise recente”.


